-
2Se mentre passeggiamo in un parco, proviamo a cimentarci con qualche attrezzo ginnico, potrebbe capitare che uno di questi sia…Spunti potenzialmente utili senza AI (AI free)29 Settembre 2024
-
2The race of research to obtain new therapeutic paths in Medicine, especially for tumor diseases, sometimes takes on a spasmodic…English Version25 Agosto 2024
-
2La corsa della ricerca per ottenere nuovi percorsi terapeutici in Medicina, soprattutto per le malattie tumorali, talora assume un ritmo…Prospettive future14 Agosto 2024
-
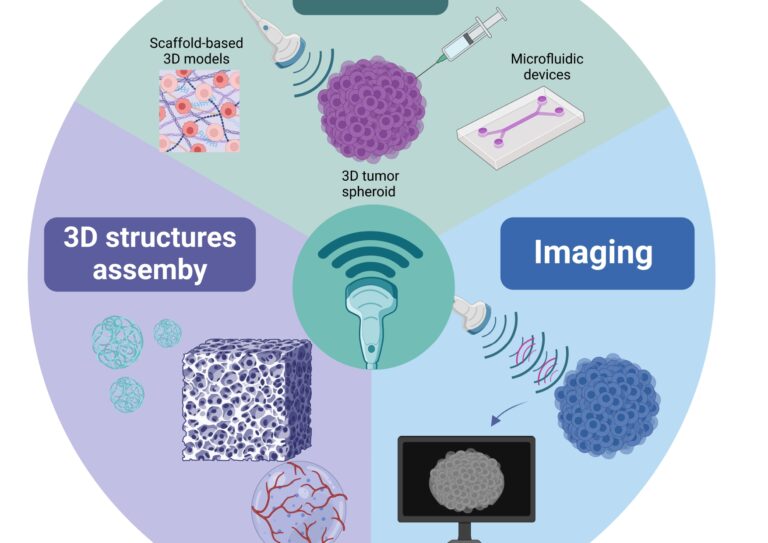
3Gli Ultrasuoni (US) sono onde pressorie acustiche che non sono percepite dall’orecchio umano e si diffondono nei tessuti che compongono…Prospettive future8 Agosto 2024
-
4Le terapie antitumorali a volte producono effetti avversi significativi sugli occhi [1,2], che possono danneggiare la vista del paziente a…Terapie e metodiche di cura4 Luglio 2024
Prospettive future
Terapia dei Linfomi: Nanoparticelle biomimetiche stimolate da Ultrasuoni.
Nanoparticelle biomimetiche e mirate come terapia stimolo-reattiva contro i Linfomi. Dr.ssa Veronica Vighetto, Prof.ssa Valentina Cauda – TNH lab del Politecnico di Torino Il linfoma di Burkitt (BL) Il linfoma di Burkitt (BL) è una neoplasia rara, particolarmente aggressiva e rapida nel suo sviluppo, che origina nei linfociti B maturi. L’incidenza è in costante aumento, […]
Nanoparticelle biomimetiche e mirate come terapia stimolo-reattiva contro i Linfomi.
Dr.ssa Veronica Vighetto, Prof.ssa Valentina Cauda – TNH lab del Politecnico di Torino
Il linfoma di Burkitt (BL)
Il linfoma di Burkitt (BL) è una neoplasia rara, particolarmente aggressiva e rapida nel suo sviluppo, che origina nei linfociti B maturi. L’incidenza è in costante aumento, e rappresenta ad oggi il 44% dei linfomi in età pediatrica, ma può colpire anche gli adulti.
Lo studio del BL ha portato all’identificazione della prima aberrazione cromosomica ricorrente nel linfoma, t(8;14)(q24;q32), e alla successiva scoperta del ruolo centrale di MYC e del virus Epstein-Barr (EBV, che provoca la Mononucleosi infettiva) nella genesi tumorale.
Storicamente sono stati riconosciuti il BL endemico, il BL sporadico non endemico e il BL associato all’immunodeficienza, ma la differenziazione di queste varianti epidemiologiche è confusa dalla frequenza della positività all’EBV [1].
La Terapia attuale
La terapia a cui sono sottoposti la maggior parte dei pazienti affetti da questo tipo di linfoma non Hodgkin è la chemioterapia che, nonostante la comprovata efficacia, risulta essere invasiva e aspecifica, danneggiando la salute del paziente e la sua qualità di vita. Gli effetti collaterali della chemioterapia sono infatti tanti e debilitanti, dalla nausea alla formazione di lividi, lesioni delle mucose e l’indebolirsi del sistema immunitario, passando attraverso il danneggiamento delle cellule sane, poiché la terapia non è in grado di distinguere il tessuto sano da quello malato.
La ricerca per una terapia sicura e con minori effetti avversi
Queste sono le ragioni che muovono la ricerca in campo oncologico verso lo sviluppo di agenti terapeutici in grado di essere efficaci, e soprattutto capaci di uccidere le cellule tumorali, risparmiando dalla loro azione tossica il tessuto sano.
In questo panorama si inserisce il gruppo della Prof.ssa Valentina Cauda, che da anni lavora per sviluppare nanotecnologie all’avanguardia per la terapia mirata di linfomi e tumori circolanti, presso il TNH lab del Politecnico di Torino, a cui mi rivolgo per conoscere gli ultimi aggiornamenti a riguardo.
Prof.ssa Cauda ci può spiegare cosa tratta questo sistema terapeutico proposto nel suo recente lavoro?
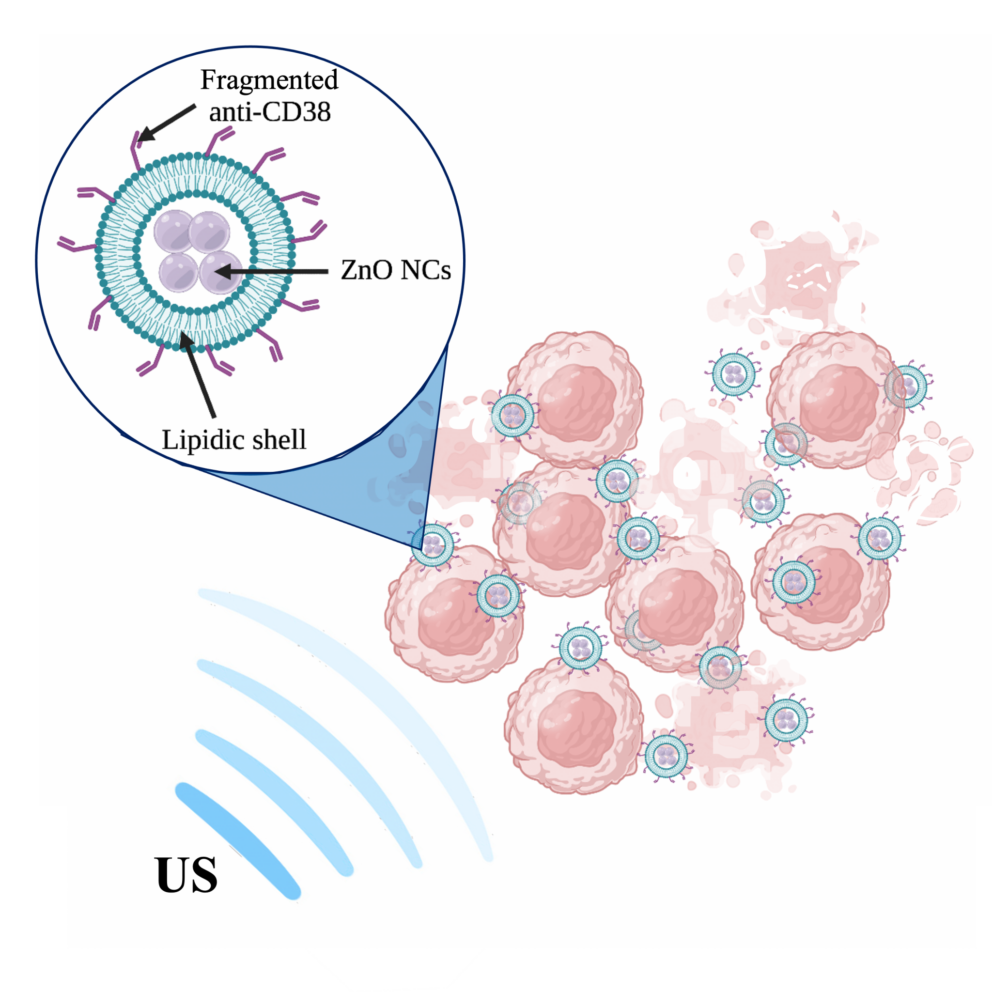
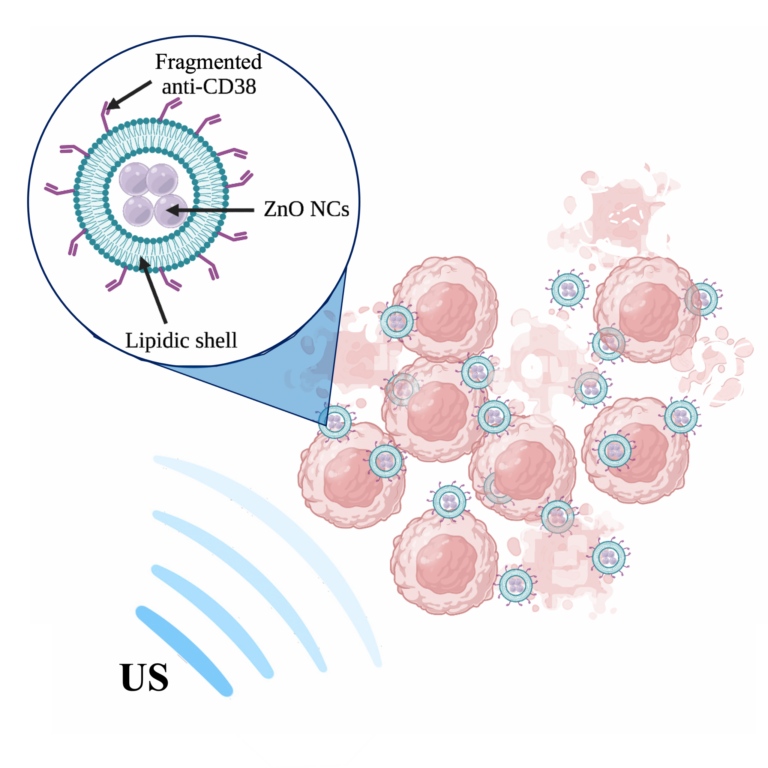
“L’agente terapeutico è una nanoparticella biomimetica ed intelligente. Il suo cuore è composto da cristalli di ossido di zinco, dalle dimensioni nanometriche, ricoperti poi da una speciale formulazione lipidica, in grado di mantenere la particella stabile nel sistema sanguigno e renderla biomimetica. Ed è proprio questo guscio lipidico esterno ad essere stato ingegnerizzato: ad esso si è legato un agente di “targeting”, cioè una molecola in grado di riconoscere le cellule tumorali del Linfoma di Burkitt, permettendo quindi alla nanoparticella di entrare in maniera preferenziale nelle cellule malate, risparmiando le sane. In particolare, per questo lavoro è stato utilizzato un frammento di anticorpo anti-CD38. La nanoparticella in sé non è tossica, ma il suo potere terapeutico può essere attivato da remoto, irradiando la zona interessata con ultrasuoni.”
Dr.ssa Veronica Vighetto, lei è primo autore della pubblicazione qui discussa, ci può dire in che modo gli ultrasuoni agiscono su queste particelle?
“Gli ultrasuoni sono largamente utilizzati in ambito clinico e non rappresentano un pericolo per la salute. Nel nostro caso abbiamo ampiamente verificato che gli ultrasuoni sono in grado di “accendere” le capacità citotossiche delle nanoparticelle da noi prodotte. Lo studio da noi pubblicato dimostra come questa nanotecnologia sia in grado, quando attivata da ultrasuoni, di avviare efficacemente il processo di morte cellulare solo nelle cellule del tumore di Burkitt, risparmiando i linfociti B sani.
L’innovazione di questa nanotecnologia non risiede esclusivamente nella sua efficacia terapeutica, ma nella sua sfaccettata potenzialità.
Lo stesso tipo di nanoparticella può essere ingegnerizzata con molecole di targeting diverse, che si dirigeranno verso diversi tipi di cellule tumorali, rendendo la nanoparticella proposta uno strumento utile per la terapia di svariati tipi di tumori.
Ed è dunque per questo motivo che nello stesso gruppo si sta valutando l’efficacia terapeutica di questa nanoparticella intelligente attivata da ultrasuoni su diversi tipi di leucemie, linfomi e sul mieloma multiplo, arrivando a testarne l’effetto in un trial clinico che si focalizza sul linfoma cutaneo a cellule T (CTC) in una particolare sotto casistica che è la Sindrome di Sezary.
Il ruolo della nanoparticella: sia terapeutico che diagnostico.
Un ulteriore importante aspetto legato alla natura di questa nanoparticella, è la sua capacità di generare luce quando stimolata con ultrasuoni. Il gruppo della Prof. Cauda ha verificato come l’ossido di zinco in nanocristalli sia in grado di aumentare il numero di fotoni, (“pacchetti di luce”), prodotti durante l’irradiazione con ultrasuoni, grazie al fenomeno della sonoluminescenza. Questa luce prodotta durante la terapia permetterebbe non solo di visualizzare la zona trattata, ma di sfruttare la nanoparticella sia agente terapeutico sia come agente diagnostico.”
La prospettiva futura
Il laboratorio della Prof.ssa Cauda dimostra come sia veloce e interdisciplinare la ricerca in campo medico e tecnologico, e traccia un percorso per lo sviluppo di nanotecnologie intelligenti e esternamente attivabili in ambito terapeutico e diagnostico, aprendo nuove possibilità per la medicina personalizzata.
Bibliografia:
[1] López C, Burkhardt B, Chan JKC, Leoncini L, Mbulaiteye SM, Ogwang MD, Orem J, Rochford R, Roschewski M, Siebert R. Burkitt lymphoma. Nat Rev Dis Primers. 2022 Dec 15;8(1):78. doi: 10.1038/s41572-022-00404-3. PMID: 365223
https://www.nature.com/articles/s41572-022-00404-3
[2] Vighetto V, Conte M, Rosso G, Carofiglio M, Sidoti Abate F, Racca L, Mesiano G, Cauda V. Anti-CD38 targeted nanotrojan horses stimulated by acoustic waves as therapeutic nanotools selectively against Burkitt’s lymphoma cells. Discov Nano. 2024 Feb 14;19(1):28. doi: 10.1186/s11671-024-03976-z. PMID: 38353903; PMCID: PMC10866835.
https://link.springer.com/article/10.1186/s11671-024-03976-z
[3] Dumontel B, Susa F, Limongi T, Vighetto V, Debellis D, Canta M, Cauda V. Nanotechnological engineering of extracellular vesicles for the development of actively targeted hybrid nanodevices. Cell Biosci. 2022 May 14;12(1):61. doi: 10.1186/s13578-022-00784-9. PMID: 35568919; PMCID: PMC9107671.
https://cellandbioscience.biomedcentral.com/articles/10.1186/s13578-022-00784-9
English Version (online at : https://tnhlab.polito.it/biomimetic-and-targeted-nanoparticles-as-a-stimuli-responsive-therapy-againstleukaemia/